質量パーセント濃度の求め方|水溶液の濃度計算【理科のコツ】
テーマ:溶解度・水溶液・再結晶
溶解度の考え方──表の読み取りと再結晶の計算まで整理しよう
溶解度は、ある温度で水100gにどれだけ物質が溶けるかを表す数値です。中学受験理科では、溶解度の意味、飽和水溶液、温度による溶ける量の変化、冷やしたときに出てくる結晶量がよく問われます。この記事では、溶解度表の読み方と水溶液計算の考え方を、例題と表で確認します。
「表の数値は読めるのに、何gの結晶が出るかで計算が進みにくい」「溶解度と濃度の違いが混ざる」という場合は、溶解度表と再結晶の計算を中学受験理科の個別指導で確認したい方はこちらから、単元の復習方法を確認できます。
動画で学ぶ:水溶液のこさと計算の土台
溶解度の問題でも、溶質・溶媒・溶液の区別が土台になります。まずは動画で水溶液の言葉と計算の考え方を確認し、そのうえで溶解度表や再結晶の問題へ進みましょう。
1. 溶解度とは?──水100gに溶ける限界の量
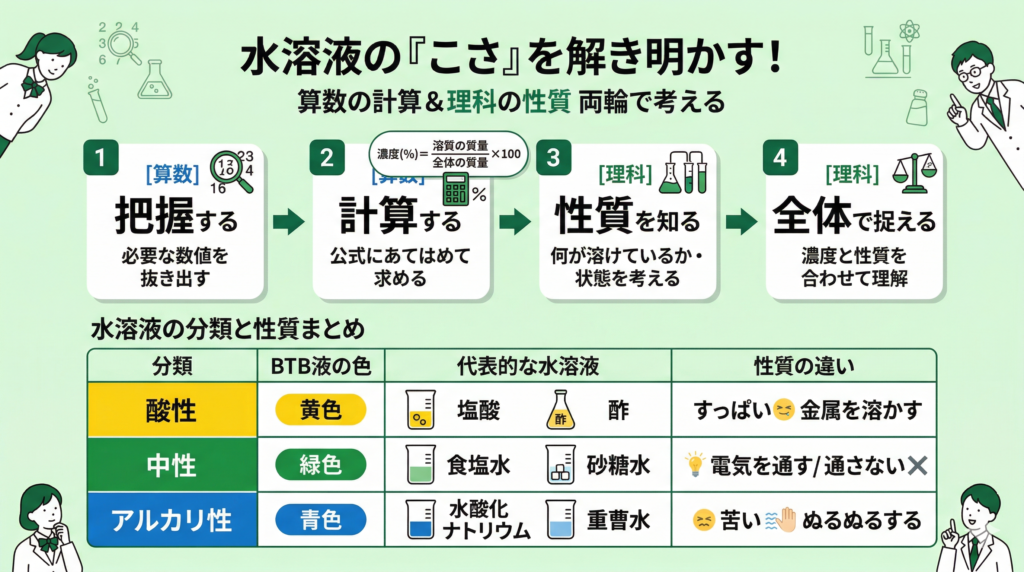
溶解度とは、ある温度で、水100gに溶ける物質の最大量を表す数値です。
- 水100gを基準にする
- 温度によって溶ける量が変わる
- それ以上溶けない状態を飽和水溶液という
たとえば、ある物質の20℃での溶解度が30gなら、20℃の水100gにはその物質が最大30gまで溶ける、という意味です。
この「最大量」という考え方が、再結晶の問題でとても重要になります。温度を下げると溶けていられる量が減り、その差が結晶として出てくるからです。
2. 溶質・溶媒・溶液の基本用語を整理しよう
溶解度の問題でも、まず確認したいキーワードは次の3つです。
溶媒・溶質・溶液の定義
- 溶媒(ようばい):
物質を溶かす側の液体(中学ではほとんど水) - 溶質(ようしつ):
溶けている物質(食塩・砂糖・ミョウバンなど) - 溶液(ようえき):
溶媒と溶質が混ざりあったできあがりの液体
具体例でイメージ
- 水に砂糖を溶かした液体 → 砂糖水(水溶液)
- このときの役割
・水 …… 溶媒
・砂糖 …… 溶質
・砂糖水 …… 溶液 - 溶解度の問題では、水100gに溶ける溶質の量を読む
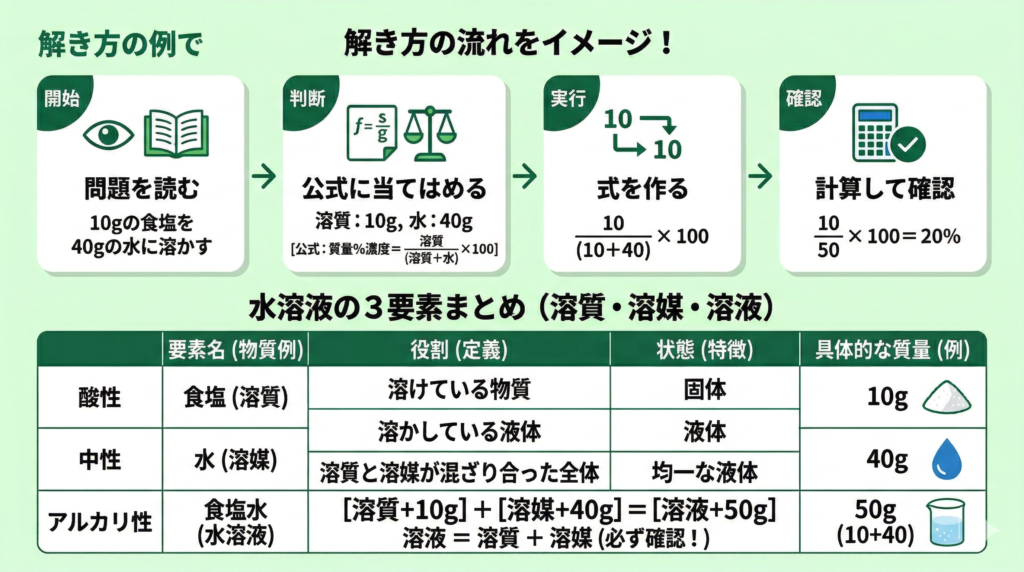
中学受験理科では、水溶液=水に物質が溶けた液体というイメージを持ち、問題文の中で水・溶けている物質・できあがった液体を分けて読むことが大切です。
3. 溶解度表の読み方──温度と溶ける量を見る
溶解度の問題では、表やグラフがよく出ます。表を見るときは、次の2つを必ず確認します。
- 何℃のときの値か
- 水100gに何g溶けるか
以下は、考え方を確認するための練習用の表です。
| 温度 | Aの溶解度 | 意味 |
|---|---|---|
| 20℃ | 30g | 20℃の水100gに、Aは最大30gまで溶ける。 |
| 60℃ | 80g | 60℃の水100gに、Aは最大80gまで溶ける。 |
この表から分かるのは、温度が高いほどAは多く溶ける、ということです。60℃で80g溶けていたAの水溶液を20℃まで冷やすと、20℃では30gまでしか溶けていられません。
したがって、80g – 30g = 50g が結晶として出てくる、と考えます。
4. 質量パーセント濃度の考え方──溶解度との違いも確認
水溶液のこさを表す方法はいくつかありますが、中学理科でよく使うのが
質量パーセント濃度です。
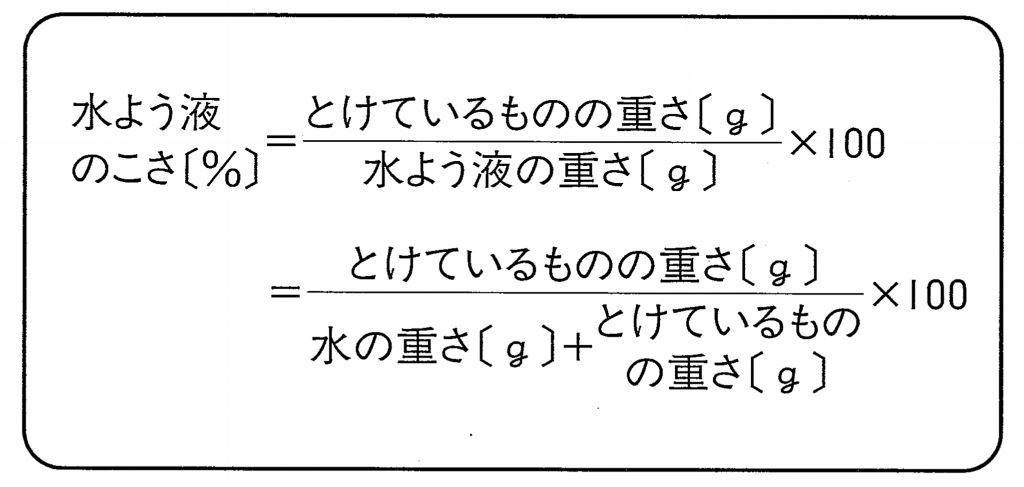
考え方の基本は、次の通りです。
- 溶液の重さ分の、溶けているものの重さを割合で表したもの
- 教科書によっては「質量」を使って(溶質の質量 ÷ 溶液の質量)× 100と書かれる
- 「溶液の質量」=溶媒の質量 + 溶質の質量
溶解度は水100gに溶ける限界量、質量パーセント濃度は水溶液全体のうち何%が溶質かを表す数値です。似ていますが、見ているものが違います。
5. 例題で確認:170gの水に30gの砂糖を溶かした水溶液
質量パーセント濃度の代表的な例題を、理科の視点で整理しておきましょう。
| 条件 | 考え方 |
|---|---|
| 条件 |
|
| 溶液の質量 |
|
| 質量パーセント濃度 |
|
ここで注目してほしいポイントは次のとおりです。
- 分母(溶液の質量)のほうが必ず大きくなる(溶質+溶媒だから)
- そのため、溶質 ÷ 溶液の値は必ず1より小さな小数になる
- 小数のままだと見づらいので、100を掛けて%に直しているだけ
溶解度の問題でも、溶質・溶媒・溶液の区別はそのまま使います。表の読み取りと濃度計算を別々にせず、水溶液単元の中でつなげて確認しましょう。
6. 再結晶の計算──冷やすと何g出てくるか
溶解度の入試問題でよく問われるのが、再結晶です。温度を下げると、溶けていられる量が少なくなり、余った物質が結晶として出てきます。
| 条件 | 考え方 |
|---|---|
| 高温で溶けていた量 | 60℃の水100gにAが80g溶けていた。 |
| 冷やした後に溶けていられる量 | 20℃ではAは30gまで溶ける。 |
| 出てくる結晶 | 80g – 30g = 50g |
この考え方は、水の量が100g以外になると少し難しくなります。たとえば水が50gなら、表の値を半分にして考える必要があります。
- 水100gに80g溶ける → 水50gなら40g溶ける
- 水100gに30g溶ける → 水50gなら15g溶ける
- 冷やすと出る結晶 → 40g – 15g = 25g
表は水100gを基準にしているため、水の量が変わったら、溶ける量も同じ割合で変えて考えます。
7. よくあるつまずきポイントと対策
溶解度と水溶液計算でよくある間違いを、あらかじめ知っておくと安心です。
① 水100gの基準を忘れる
- 溶解度は水100gに溶ける量
- 水が50gなら表の数値を半分にする
- 水が200gなら表の数値を2倍にする
② 溶解度と濃度を同じものとして扱う
- 溶解度=水100gに溶ける限界量
- 質量パーセント濃度=水溶液全体のうち溶質が何%か
- 表の問題か、割合の問題かを先に見る
③ 再結晶で差を取れない
- 高温で溶けていた量を確認する
- 低温で溶けていられる量を確認する
- 差を取ると、出てくる結晶量になる
④ 問題文の言い換えで混ざる
- 溶けている物質=溶質
- 水=溶媒
- できあがった液体=溶液
- 温度変化があれば溶解度表を使う
計算自体は算数の練習でスムーズになります。理科では、どの表を使うのか、どの量を比べるのかを読み取る力を鍛えていきましょう。
8. 溶解度と水溶液のまとめ表
ここまでの内容を、確認しやすいように表に整理しました。
| ポイント | 内容 |
|---|---|
| 溶解度 |
|
| 飽和水溶液 |
|
| 再結晶 |
|
| 質量パーセント濃度 |
|
| 重要キーワード |
|
水溶液のこさだけでなく、溶解度・中和・気体まで含めて化学分野全体の弱点を見直したいときは、中学受験理科の化学分野の全体像はこちらも役立ちます。
9. 確認クイズ(10問)で理解をチェック!
ここまで学んだ内容を、10問のクイズで確認してみましょう。
各問題の「正解を見る」ボタンを押すと答えが表示され、ボタンは消えます。
| 問題 | 選択肢 | 正解を見る |
|---|---|---|
| 1. 溶解度とは何を表す数値ですか? | A. 水溶液全体の重さ B. 水100gに溶ける物質の最大量 C. 溶液の温度 D. 溶質の色 |
|
| 2. それ以上物質が溶けない水溶液を何といいますか? | A. 飽和水溶液 B. 蒸留水 C. 濃塩酸 D. 石灰水 |
|
| 3. 溶媒とは何を指しますか? | A. 溶けている物質 B. 物質を溶かす液体 C. 固体部分 D. 出てきた結晶 |
|
| 4. 溶質とは何を指しますか? | A. 溶けている物質 B. 水 C. 水溶液全体 D. 温度 |
|
| 5. 溶解度表の基準になる水の量はどれですか? | A. 1g B. 10g C. 100g D. 1000g |
|
| 6. 高温の水溶液を冷やして結晶が出ることを何といいますか? | A. 中和 B. 再結晶 C. 蒸発 D. 沈降 |
|
| 7. 60℃で80g、20℃で30g溶ける物質を水100gに溶かし、60℃から20℃に冷やすと何g出ますか? | A. 20g B. 30g C. 50g D. 80g |
|
| 8. 質量パーセント濃度の公式はどれですか? | A. (溶媒の質量 ÷ 溶液の質量)× 100 B. (溶質の質量 ÷ 溶液の質量)× 100 C. (溶液の質量 ÷ 溶質の質量)× 100 D. (溶液の質量 ÷ 溶媒の質量)× 100 |
|
| 9. 溶液の質量の計算方法として正しいのはどれですか? | A. 溶質の質量 B. 溶媒の質量 C. 溶質 + 溶媒の質量 D. 溶質 ÷ 溶媒の質量 |
|
| 10. 溶解度と質量パーセント濃度の違いとして正しいものは? | A. どちらも同じ数値を表す B. 溶解度は水100gに溶ける量、濃度は溶液全体に対する溶質の割合 C. 溶解度は温度と関係しない D. 濃度は溶質と関係しない |
10. まとめ──溶解度は「水100gに何g溶けるか」で読む
- 溶解度は、ある温度で水100gに溶ける物質の最大量を表す。
- 飽和水溶液は、その温度でそれ以上物質が溶けない水溶液のこと。
- 溶解度表は、何℃で何g溶けるかを読む。
- 冷やしたときに出る結晶量は、高温で溶けていた量と低温で溶ける量の差で考える。
- 水の量が100g以外なら、表の値も同じ割合で変えて考える。
- 質量パーセント濃度は、溶液全体に対する溶質の割合なので、溶解度とは区別する。
溶解度の問題は、暗記だけではなく、表を読む力と割合計算が必要です。表の数値を見て、どの温度で何g溶けるのか、冷やすと何g出るのかを言葉で説明できるようにしていきましょう。
水溶液のこさを含む化学分野の整理を一歩先まで進めたいなら、次のページも参考になります。
溶解度・中和・気体まで化学分野をまとめて確認したい人へ
「溶解度表は読めるけれど、再結晶の計算になると不安」「水溶液・中和・気体の性質まで化学分野をまとめて復習したい」という人は、
化学分野を単元ごとに確認していくのがおすすめです。
- 溶質・溶媒・溶液から溶解度表までの整理
- 再結晶・濃度計算・実験問題の演習
- 動画+問題演習での復習サポート
受験理科専門塾「しゅん吉クエスト」では、理科を「苦手」から「得意」に変えるためのサポートを行っています。


